微生物组测序数据清洗,从原始数据到高质量分析
- 开题报告
- 2025-04-03 02:57:52
- 9
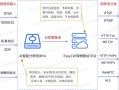
微生物组测序数据清洗是从原始测序数据中去除低质量序列、污染和噪音,以获得高质量数据的关键步骤,该过程通常包括质量控制、去冗余、去宿主序列、去除接头和引物序列等环节,使用FastQC等工具评估原始数据质量,随后通过Trimmomatic或Cutadapt等软件去除低质量碱基、接头序列和短读长,对于宿主污染(如人类基因组),可采用Bowtie2等比对工具进行过滤,还需通过去冗余和嵌合体检测(如UCHIME)进一步提高数据可靠性,经过清洗的高质量数据可用于后续的物种注释、功能预测和多样性分析等研究,这一流程对确保微生物组研究的准确性和可重复性至关重要。
微生物组(Microbiome)研究近年来在医学、环境科学和农业等领域取得了重要进展,高通量测序技术(如16S rRNA测序或宏基因组测序)能够快速获取样本中的微生物群落信息,但原始测序数据往往包含噪声、低质量序列和污染,直接影响后续分析的准确性。数据清洗(Data Cleaning) 是微生物组分析的关键步骤。
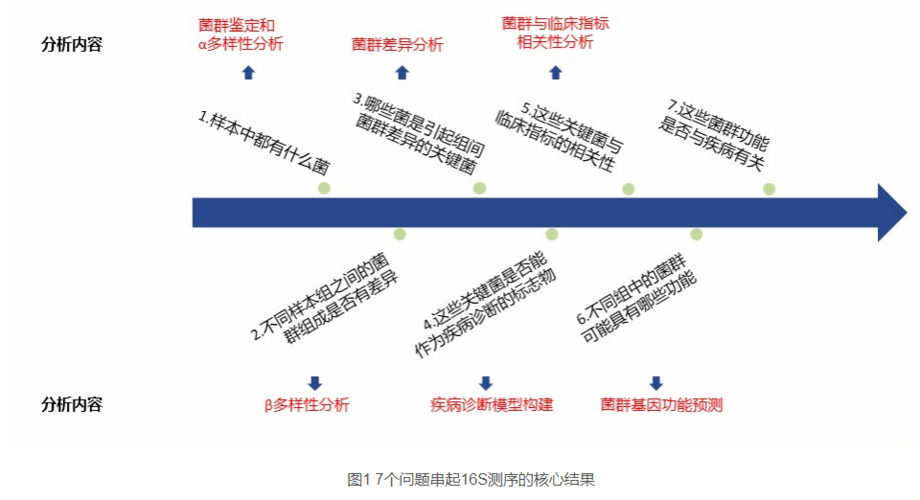
本文将介绍微生物组测序数据清洗的基本流程,帮助初学者理解如何从原始数据中提取高质量信息,为后续的物种注释、功能预测和统计分析奠定基础。
原始数据格式与常见问题
微生物组测序数据通常以 FASTQ 格式存储,包含测序序列(Reads)及其对应的质量分数(Quality Scores),常见的数据质量问题包括:
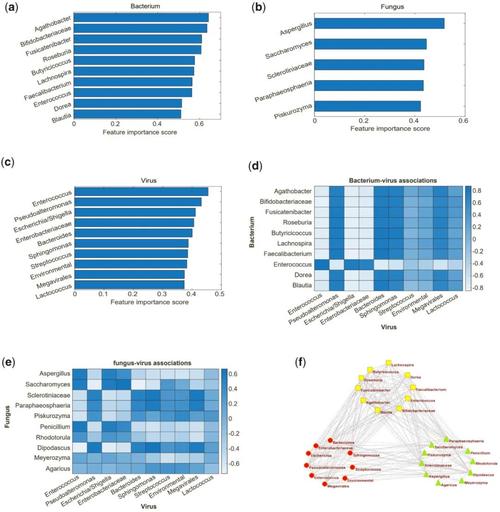
- 低质量碱基(Low-quality bases):测序过程中可能产生错误碱基,影响序列比对和注释。
- 接头污染(Adapter contamination):测序过程中残留的引物或接头序列。
- 嵌合体(Chimeras):PCR扩增时产生的非目标序列。
- 宿主污染(Host contamination):如人类肠道微生物组测序中可能混入人类DNA。
数据清洗流程
微生物组测序数据清洗通常包括以下步骤:
(1)质量评估(Quality Control)
使用工具(如 FastQC)检查原始数据的质量分布,包括:
- 每个碱基的质量分数(Phred Score):一般要求Q30(错误率≤0.1%)以上。
- 序列长度分布:过短或过长的序列可能有问题。
- GC含量异常:某些微生物的GC含量异常可能表明污染。
示例命令(FastQC):
fastqc raw_data.fastq -o output_dir/
(2)去接头与低质量序列过滤
使用 Cutadapt 或 Trimmomatic 去除接头序列并过滤低质量Reads:
- 去除测序接头(Adapter)
- 截断低质量碱基(如Q<20)
- 丢弃过短序列(如长度<50bp)
示例命令(Cutadapt):
cutadapt -a ADAPTER_SEQ -q 20 -m 50 -o cleaned.fastq raw_data.fastq
(3)去宿主污染(Host Removal)
如果样本来自人体或动物(如肠道、皮肤微生物组),可能需要去除宿主DNA,常用工具:
- Bowtie2(比对宿主基因组并去除匹配序列)
- KneadData(自动化去宿主流程)
示例命令(Bowtie2):
bowtie2 -x host_genome -U cleaned.fastq --un non_host.fastq > host_mapped.sam
(4)去重复序列(Dereplication)
PCR扩增可能导致相同序列被多次测序,可使用 VSEARCH 或 USEARCH 去除冗余序列:
vsearch --derep_fulllength input.fasta --output unique.fasta --sizeout
(5)嵌合体去除(Chimera Removal)
嵌合体(Chimeras)是PCR扩增时产生的假序列,需用 UCHIME 或 VSEARCH 检测并去除:
vsearch --uchime_denovo unique.fasta --nonchimeras final.fasta
(6)OTU/ASV聚类(可选)
- OTU(Operational Taxonomic Unit):基于97%相似度聚类(如 USEARCH)。
- ASV(Amplicon Sequence Variant):更精确的序列变异识别(如 DADA2、Deblur)。
示例(DADA2 in R):
library(dada2) filtered <- filterAndTrim(raw_reads, filtered_reads, maxN=0, maxEE=2, truncQ=2) derep <- derepFastq(filtered_reads) dada <- dada(derep, err=learnErrors(derep)) seqtab <- makeSequenceTable(dada)
数据清洗后的验证
清洗后的数据应再次进行质量检查,确保:
- 平均质量分数达标(Q30+)。
- 序列长度符合预期(如16S V4区~250bp)。
- 嵌合体比例<1%。
- 宿主污染基本去除(如人类DNA残留<0.1%)。
工具推荐:
- MultiQC(整合FastQC、Cutadapt等报告)
- Kraken2(快速检测污染物种)
常见问题与优化建议
- 问题1:数据丢失过多? → 调整过滤阈值(如放宽Q值或最小长度)。
- 问题2:嵌合体比例高? → 优化PCR条件或使用更严格的去嵌合体方法。
- 问题3:计算资源不足? → 使用云计算(如AWS、Google Cloud)或降低数据量(随机抽样)。
微生物组测序数据清洗是确保分析可靠性的关键步骤,本文介绍了从原始FASTQ数据到高质量序列的标准流程,包括:
- 质量评估(FastQC)
- 去接头与过滤(Cutadapt/Trimmomatic)
- 去宿主污染(Bowtie2/KneadData)
- 去嵌合体(UCHIME/VSEARCH)
- OTU/ASV聚类(DADA2/USEARCH)
通过严格的清洗流程,可以提高后续物种注释、α/β多样性分析和功能预测的准确性,希望这篇指南能帮助初学者更好地处理微生物组数据!
参考文献与工具推荐
- Andrews, S. (2010). FastQC.
- Martin, M. (2011). Cutadapt.
- Callahan, B. J. (2016). DADA2.
- Edgar, R. C. (2010). UCHIME.
如果你有疑问或建议,欢迎留言讨论! 🚀
本文由Renrenwang于2025-04-03发表在人人写论文网,如有疑问,请联系我们。
本文链接:http://www.renrenxie.com/ktbg/123.html